BrightGene Sajikan Data Fase 2 yang Positif untuk Agonis Ganda GLP-1R/GIPR untuk Pengelolaan Berat Badan dan Diabetes Tipe 2
- Selasa, 24 Juni 2025 10:24 WIB
- waktu baca 6 menit

- Data Fase 2 menyoroti potensi terbaik di kelasnya dari agonis ganda GLP-1R/GIPR BGM0504 untuk pengelolaan berat badan dan pengurangan risiko metabolik pada individu dengan diabetes tipe 2 dan individu kelebihan berat badan non-obesitas
- Data praklinis untuk BGM1812 mendukung pengembangan lebih lanjut sebagai analog amylin generasi berikutnya untuk pengobatan obesitas
Suzhou, China, (ANTARA/PRNewswire)- BrightGene Pharmaceutical Co., Ltd., perusahaan farmasi internasional yang didorong oleh inovasi, mempresentasikan data dari dua studi Fase 2 untuk BGM0504, agonis ganda yang sedang diselidiki yang menargetkan reseptor glukagon-like peptide-1 (GLP-1R) dan reseptor glucose-dependent insulinotropic polypeptide (GIPR), bersama dengan data praklinis untuk analog amylin barunya, BGM1812, pada Konferensi Ilmiah ke-85 Asosiasi Diabetes Amerika (ADA).
Hasil dari dua studi Fase 2 yang terpisah untuk BGM0504 menunjukkan potensi yang signifikan untuk pengelolaan berat badan dan pengurangan risiko metabolik pada individu dengan diabetes tipe 2 (termasuk keunggulan dibandingkan semaglutide), serta pada individu kelebihan berat badan dan obesitas yang tidak menderita diabetes. Data praklinis untuk BGM1812 menunjukkan aktivasi reseptor yang unggul, penurunan berat badan yang kuat dan potensi sinergis dengan agonisme ganda GLP-1/GIP, mendukung pengembangannya sebagai analog amylin generasi berikutnya untuk pengobatan obesitas.
“Data Fase 2 ini menyoroti potensi luar biasa dari BGM0504 sebagai pengobatan untuk diabetes tipe 2 dan obesitas, termasuk potensi keunggulan dibandingkan semaglutide dan profil keamanan yang kuat, sementara data praklinis kami untuk BGM1812 mendukung pengembangan berkelanjutan sebagai analog amylin generasi berikutnya untuk pengobatan obesitas, menekankan potensi tambahan dalam portofolio kami,” kata Dr. Jiandong Yuan, CEO BrightGene. “Dengan memanfaatkan keahlian luas kami dalam peptida dan warisan kuat dalam pengembangan obat yang efisien dan berkualitas tinggi, BrightGene berkomitmen untuk mempercepat terapi inovatif untuk membantu mengatasi kebutuhan pasien yang belum terpenuhi dalam penyakit metabolik dan area terapeutik penting lainnya.”
Studi Fase 2 BGM0504 pada Diabetes Tipe 2
Studi multicenter, acak, double-blind (kontrol plasebo) dan open-label (kontrol positif semaglutide) ini mengevaluasi farmakokinetik, keamanan, dan kemanjuran injeksi subkutan mingguan BGM0504 berdasarkan titik akhir utama yaitu perubahan HbA1c dari baseline pada Minggu ke-12 pemberian dosis target, serta berbagai titik akhir sekunder termasuk PPG-2 jam, FPG, berat badan, HbA1c dan proporsi target gabungan HbA1c/berat badan, HOMA2-B, lipid darah, tekanan darah sistolik (SBP) dan tekanan darah diastolik (DBP).
Studi ini melibatkan 67 partisipan dengan diabetes tipe 2 berusia antara 18 dan 65 tahun, di mana 64 partisipan menerima dosis setelah randomisasi, dan mereka kemudian dibagi secara acak ke dalam lima kelompok: 5mg (n=13), 10mg (n=12), 15mg (n=13), kelompok kontrol positif (semaglutide; n=16) atau plasebo (n=13). Peserta yang direkrut adalah orang dewasa dengan HbA1c awal antara 7,0% dan 10,0%, serta indeks massa tubuh (BMI) antara 19,5 dan 35 kg/m2.
Pada Minggu ke-12 pemberian dosis target, pengobatan dengan BGM0504 menghasilkan penurunan HbA1c di ketiga kelompok dosis yang secara statistik signifikan dibandingkan dengan kelompok plasebo dan lebih besar dibandingkan dengan pengobatan semaglutide, termasuk -1,72% pada kelompok dosis 5mg, -1,94% pada kelompok dosis 10mg, dan -2,48% pada kelompok dosis 15mg, dibandingkan dengan -1,43% pada semaglutide dan -0,28% pada plasebo. Hasil serupa diamati dalam berbagai titik akhir sekunder, termasuk PPG-2 jam, FPG, berat badan, dan HbA1c dan proporsi target gabungan HbA1c/berat badan, sementara tren perbaikan yang bervariasi diamati dalam HOMA2-B, lipid darah, SBP, dan DBP. Sebagian besar kejadian efek samping yang muncul selama pengobatan (TEAE) adalah Grade 1 atau 2 selama tahap titrasi cepat dan secara bertahap dapat ditoleransi setelah mencapai dosis target. Efek samping gastrointestinal yang paling umum terkait pengobatan adalah diare, mual, dan perut kembung; tidak ada reaksi hipoglikemia atau efek samping tak terduga lainnya yang terjadi.
Studi Fase 2 BGM0504 dalam Obesitas
Studi acak, double-blind, terkontrol plasebo ini mengevaluasi keamanan dan efektivitas BGM0504 pada 120 orang dewasa Tiongkok dengan obesitas selama pemberian dosis ganda (injeksi subkutan). Peserta yang direkrut adalah orang dewasa dengan BMI ≥ 24kg/m2 (rata-rata BMI saat pendaftaran ≥ 27kg/m2) dengan pradiabetes dan/atau setidaknya satu komorbiditas terkait obesitas, atau orang dewasa dengan obesitas (BMI ≥ 28kg/m², rata-rata BMI saat pendaftaran ≥ 30kg/m²). Peserta diacak ke dalam empat kelompok: 5 mg (n=30), 10 mg (n=30), 15 mg (n=30), atau plasebo (n=30). Studi ini terdiri dari fase titrasi (2-6 minggu), pengobatan selama 24 minggu dengan pemberian dosis mingguan, dan masa tindak lanjut selama 2 minggu.
Hasil studi menunjukkan pengurangan lingkar pinggang mulai dari −8,0 cm hingga −12,98 cm (p < 0,001), dan penurunan berat badan yang signifikan mulai dari -10,77% hingga -19,78% (rata-rata LS, disesuaikan terhadap plasebo). Hasil juga menunjukkan peningkatan tekanan darah sistolik mulai dari −11,60 hingga −13,03 mmHg dan tekanan darah diastolik mulai dari −5,98 hingga −7,50 mmHg (p < 0,05).
Hasil sekunder lebih lanjut mendukung efektivitas BGM0504, dan semua dosis dapat ditoleransi dengan baik dengan efek samping yang umum.
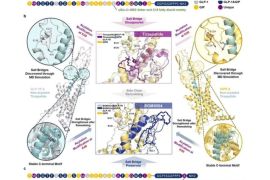
Studi Praklinis BGM1812
Dalam studi praklinis, BGM1812 menunjukkan aktivasi reseptor yang kuat dengan peningkatan aktivitas agonis sebesar 1,8× dan 2,2× (EC50) masing-masing pada reseptor amylin dan kalsitonin dibandingkan dengan petrelintide. Agonis ini juga menunjukkan penurunan berat badan yang tergantung dosis dalam rentang dosis 0,012 – 0,12 mg/kg pada model tikus obesitas akibat diet (DIO).
Pada dosis 0,04 mg/kg, BGM1812 mencapai penurunan berat badan yang lebih besar dibandingkan petrelintide, yang sedang dikembangkan oleh Zealand Pharma. Selain itu, BGM1812 secara signifikan mempertahankan massa otot tanpa lemak relatif sambil mengurangi massa lemak relatif. Selain itu, kombinasi BGM1812 dan BGM0504 menghasilkan penurunan berat badan yang lebih besar dan lebih berkelanjutan dibandingkan kombinasi semaglutide+cagrilintide atau amycretin dalam model tikus DIO.
Tentang BGM0504
Injeksi obat hipoglikemik peptida BGM0504 adalah agonis ganda dari reseptor GLP-1 (glucagon-like peptide 1) dan GIP (glucose-dependent insulinotropic polypeptide) yang dikembangkan secara independen oleh BrightGene. BGM0504 dapat merangsang jalur hilir dari GIP dan GLP-1, menghasilkan efek biologis seperti mengontrol gula darah, mengurangi berat badan dan mengobati steatohepatitis non-alkohol (NASH), dan menunjukkan potensi untuk pengobatan berbagai penyakit metabolik. BGM0504 saat ini berada dalam uji coba Fase 3 di Tiongkok untuk manajemen berat badan dan diabetes tipe 2 serta telah menyelesaikan studi penghubung Fase 1 untuk manajemen berat badan di AS. Hingga saat ini, BGM0504 telah diteliti pada lebih dari 1.000 pasien dan menunjukkan kemanjuran yang superior serta profil keamanan yang kuat.
Tentang BGM1812
BGM1812 adalah analog amylin baru yang dirancang menggunakan optimisasi berbasis AI/ML untuk meningkatkan aktivitas agonis dan sifat formulasi. Sebagai amylin yang kuat dan sangat tahan lama, BGM1812 berpotensi menjadi tablet oral mingguan.
Tentang BrightGene
BrightGene adalah perusahaan farmasi internasional yang didorong oleh inovasi, terdaftar di Bursa Efek Shanghai, yang didedikasikan untuk mengembangkan dan memproduksi terapi berkualitas tinggi untuk memenuhi kebutuhan pasien yang belum terpenuhi. Didirikan pada tahun 2001, BrightGene telah berkembang dari pemimpin global yang mapan dalam generik dan biosimilar dengan hambatan tinggi menjadi pengembang terapi inovatif untuk penyakit metabolik dan pernapasan. Sebagai pemimpin yang mapan dalam kimia kompleks dan konjugasi, BrightGene memiliki platform mutakhir yang eksklusif dalam peptida, siRNA, nanobody, serta formulasi canggih, dan 272 paten. Perusahaan ini tetap menjadi pemasok global untuk 15 API dan 2 produk obat ke AS dan UE. BrightGene berkantor pusat di Tiongkok. Informasi tambahan tersedia di https://www.bright-gene.com/.
SOURCE Bright Gene
Pewarta: PR Wire
Editor: PR Wire
Copyright © ANTARA 2025
Dilarang keras mengambil konten, melakukan crawling atau pengindeksan otomatis untuk AI di situs web ini tanpa izin tertulis dari Kantor Berita ANTARA.
Komentar
Berita Terkait
Mengembalikan kejayaan gambir Indonesia
- 14 Juni 2025
Rekomendasi lain
Daftar lengkap tim peserta Serie A musim 2024/2025
- 11 September 2024
Urutan lengkap ibadah haji, dari ihram sampai tawaf wada
- 18 September 2024
Asal-usul sejarah Hari Pahlawan 10 November 1945 dan tujuannya
- 6 November 2024
Syarat dan biaya masuk SMA Taruna Nusantara Magelang
- 24 Oktober 2024
Sinopsis film Netflix: “Setetes Embun Cinta Niyala”
- 1 Maret 2025
Panduan tukar uang baru di kas keliling Bank Indonesia dan bank umum
- 26 Februari 2025
Keuntungan dan potensi kerugian Indonesia gabung BRICS
- 10 Januari 2025
Daftar aplikasi main saham terbaik
- 16 September 2024